Au départ, il y a une idée… mais pour la transformer en produit commercialisable, le chemin peut être long. Comment réussir ce parcours qui sépare une innovation de sa mise sur le marché ? C’était justement le thème du premier webinar organisé par Selha Group le 25 juin dernier. Retour sur les réponses clés apportées par nos trois experts : Sarah Traboulsi Delaporte, ingénieur en génie biomédical, docteur en biophysique et expert en dispositifs médicaux, Gilles Rossignol, Responsable développement d’affaires secteur médical chez Selha Group, et Dr Kleinsinger, docteur, fondateur et dirigeant de Synthebio.
De l’idée au produit :
les étapes clés du développement d’un dispositif médical
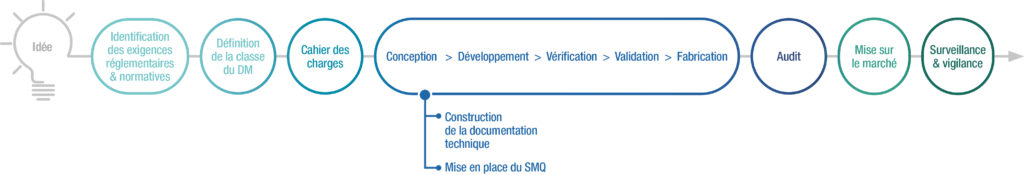
Le chemin qui sépare l’idée du produit est complexe et sinueux. Définition des exigences (réglementation, normes applicables, classification…), conception et prototypage, études cliniques & validation, documentation technique, marquage CE, industrialisation, fabrication en série… autant de jalons à franchir pour mettre au point un dispositif médical. Avoir une vision globale de ce parcours, dès le début du projet, permet de mieux appréhender les étapes décisives et d’anticiper en amont la certification du dispositif médical (marquage CE) & sa mise sur le marché.
💡 Les conseils de nos experts :
- Déterminer la nature du dispositif médical (classe I, IIa, IIb ou III)
- Identifier l’ensemble des exigences réglementaires applicables
- Rédiger un cahier des charges détaillé
- S’entourer de partenaires spécialisés dans chaque domaine (propriété intellectuelle, réglementaire, conception, fabrication…)
Pour en savoir plus, demandez le replay du webinar 👇